-
II. Applications dans le domaine de la médecine
II. Applications dans le domaine de la médecine
Après la révolution, liée au décodage du génome humain et à l’identification des protéines codées par ces gènes, l’homme fait face à un nouveau défi.
La nanomédecine est l’application des nanotechnologies au domaine médical. Elle regroupe de nombreuses branches tant par les techniques utilisées que par les domaines ciblés. L'élément phare de la nanomédecine et qui reste souvent l’image qu’on se fait des nanotechnologies, est le nanorobot. Bien que cet édifice nanométrique fasse encore rêver, les technologies utilisées aujourd’hui ne permettent pas de créer des robots en grande quantité, au vu de la complexité de leur assemblage et des risques qu’ils pourraient faire courir aux patients.

Fig. 15 : Représentation fictive d'un nanorobot saisissant un virus.
 Fig. 16 : Représentation fictive d'un nanorobot gérant la connexion entre des neurones.
Fig. 16 : Représentation fictive d'un nanorobot gérant la connexion entre des neurones.La nanomédecine, c’est aussi la recherche et l’innovation combiné au monde du nano pour vaincre les maladies les plus graves comme les troubles quotidiens. Elle doit fournir les outils d’analyse de la fonction des molécules dans l’organisme vivant et permettre de mieux comprendre certaines maladies, développer de nouvelles thérapies et des outils diagnostiques. Nous allons voir ci-dessous quelques exemples de prototypes dans le domaine de la nanomédecine et leur mode d’action, lié avec les nanoparticules présentées dans la première partie, à savoir les nanotubes de carbone et la particule ferromagnétique.
1) Les nanoparticules ferromagnétiques pour la lutte contre le cancer
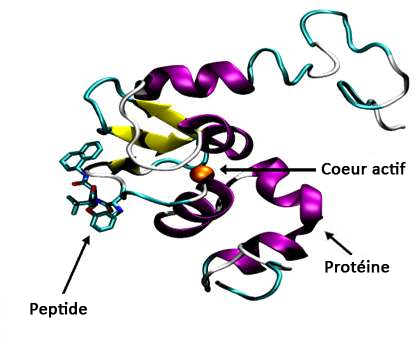
Fig. 17 : Liaison entre le peptide d'une nanoparticule et une protéine.
L’utilisation principale des nanoparticules ferromagnétiques se fait dans la lutte contre le cancer.
Les cellules cancéreuses, par exemple celles du cancer du sein, libèrent une protéine (Rho B) spécifique à ce cancer. Il suffit donc d’implémenter des récepteurs à cette protéine sur la base de la nanoparticule pour qu’elle soit capable de se fixer sur les cellules cancéreuses.
L’accumulation de cette particule dans une tumeur permettra une meilleure visualisation de celle-ci par IRM.
En effet, les appareils à IRM (Imagerie par Résonance Magnétique) sont capables de détecter les particules de fer dans l’organisme. Il devient donc possible de localiser un cancer lorsque sa taille est très réduite et avant les premiers symptômes. Cette particule peut ainsi servir d’outil pour le dépistage de certains cancers meurtriers dans le monde. On parle de médicament vectorisé, capable de choisir une cible précise.
De plus, les nano-objets peuvent être utilisés comme sources locales de chaleur : l’application d’un champ magnétique alternatif génère une augmentation de température au sein de la tumeur, ce qui la sensibilisera alors à toute attaque. L’efficacité de la chimio- ou de la radiothérapie sera ainsi améliorée sans avoir à augmenter la dose et sans augmenter les effets secondaires.
Le défi est d’obtenir pour ces nano-objets une forte sélectivité envers la tumeur et une "efficacité magnétique" sans précédent qui soit préservée tout au long du traitement. Des tests in vitro et in vivo seront réalisés en IRM et en hyperthermie pour quantifier leur efficacité.
2) Les nombreuses utilisations du nanotube de carbone
a. Transport et détection de protéines
La structure particulière du nanotube de carbone peut être utilisée pour transporter des particules.
Les nanotubes de carbone présentent un espace interne pouvant contenir de très nombreuses molécules de taille relativement importantes. Ainsi il a été imaginé d’utiliser les nanotubes comme
des "boîtes" permettant d’assurer le transport de médicaments. Par ailleurs, sur sa structure externe peuvent être accrochées différentes molécules ou corps physiques qui interagiraient avec d’autres cellules comme, par exemple, des cellules malades. Ceci permet alors de transporter sur un lieu précis les produits contenus dans le nanotube.

Fig. 18 : Liaison d'une protéine à un nanotube de carbone.
Des chercheurs du Jefferson Medical Center et de l’Université de Delaware ont mis au point un test de détection des cellules cancéreuses à l’aide de nanotubes de carbone. Leur système est composé d’électrodes métalliques polarisant des nanotubes dont la surface a été greffée avec des anticorps spécifiques de l’antigène GF1R4. Cet antigène est présent dans certaines cellules cancéreuses.
Le principe de détection repose sur le contrôle du courant qui circule dans les nanotubes polarisés : on observe une augmentation subite de courant lorsqu’une liaison anticorps-antigène se forme, et uniquement dans ce cas, ils ont observé que l’intensité d’un courant circulant dans les nanotubes préalablement polarisés augmente d’une manière très nette. Ils ont ainsi pu mettre en évidence la présence de ces cellules cancéreuses.
b. Un autre moyen de transport : la nano-aiguille
Un groupe de chercheurs de l’université de l’Illinois a réalisé une nano-aiguille utilisable à l'échelle d'une seule cellule. Elle permet d'y injecter un petit nombre de molécules, mais aussi de sonder le cytoplasme et le noyau.
L’un des rêves de la nanomédecine est de pouvoir agir directement au niveau des cellules individuelles d’un corps humain, en particulier ses neurones, à l’aide de nanorobots.
La nano-aiguille est composée d'un tube de nitrure de bore de 50 nanomètres de diamètre (équivalent au nanotube de carbone) ainsi que d'une fine couche d'or sur laquelle on fixe de une à quelques molécules seulement. Elles se libèrent facilement une fois l'aiguille insérée dans le cytoplasme.
On peut aussi injecter directement des nanoparticules magnétiques ou des boîtes quantiques, ce que les chercheurs ont fait comme ils l’expliquent dans une publication de Nano Letters. Il a ainsi été possible de suivre le métabolisme d'une cellule en repérant la fluorescence de la boîte quantique utilisée.

Fig. 19 : Schématisation de l'utilisation de la nano-aiguille.
Avec cette nano-aiguille, les chercheurs peuvent non seulement contrôler, surveiller et enregistrer comme jamais auparavant le processus de livraison de molécules actives à l’intérieur d’une cellule, mais ils peuvent aussi utiliser cette aiguille comme sonde électrochimique et biocapteur optique.
Il devient possible de suivre de façon plus fine les interactions entre protéines et molécules d’ADN et d’ARN à l'intérieur même de la cellule.

Fig. 20 : Evolution d'une boîte quantique luminescente dans une cellule.
c. Détruire des cellules : la nanobombe et les ondes radio
Le concept de la nanobombe contre le cancer est né grâce à des chercheurs américains qui ont créé un traitement à base de nanotubes de carbone s’introduisant dans une tumeur et dégageant une chaleur suffisante pour provoquer la destruction de la cellule. En effet, il serait possible d'utiliser des agrégats de nanotubes de carbone pour provoquer leur explosion à l'échelle nanométrique.
Lorsqu’on illumine un agglomérat de nanotubes, la quantité de chaleur dégagée est importante et ne peut se dissiper rapidement.
Cette équipe de chercheurs a montré qu’il était possible de contrôler ce mécanisme en solution aqueuse saline. Elle a donc suggéré de l’utiliser pour détruire localement et sélectivement des cellules cancéreuses sur lesquelles on aurait accroché ces agglomérats, qualifiés de nanobombes.
Des petites bombes à l’échelle du nanomètre peuvent être réunies en forme de grappe. Une fois exposées à la chaleur du rayonnement d’une source lumineuse, les nanobombes explosent les unes après les autres. Une autre méthode visant la destruction des cellules cancéreuses est l’utilisation des ondes radio.
Le principe consiste à introduire des nanotubes dans un organe malade, de les diriger vers les cellules cancéreuses. Ensuite, il suffit de faire passer des ondes radio à travers le tissu. Les nanotubes vont alors chauffer et détruire la tumeur, tout en épargnant les cellules non traitées.

Fig. 21 : Explosion d'une plaque de nanotubes de carbone au laser.
L’expérience a été réalisée sur le foie d’un lapin. La tumeur a été totalement irradiée mais certains tissus hépatiques sains de 2 à 5 millimètres ont subit quelques dommages, causés par la chaleur. Cependant, cibler uniquement les cellules cancéreuses est un défi majeur. Des recherches sont en cours pour tenter de combiner la détection d’un antigène spécifique à l’aide d’un nanotube et son échauffement par ondes radio.
d. Transporter des médicaments

Fig. 22 : Atomes de tritium dans un nanotube de carbone.
La structure du nanotube de carbone permet d’y fixer, à l’extérieur, des molécules ayant une affinité avec les cellules cibles pour permettre une reconnaissance précise. À l’intérieur, des médicaments ou des toxines peuvent être placés. Ils auront pour action de se mettre en contact avec une cellule malade et de délivrer au bon endroit les médicaments qui permettront de la traiter.

Fig. 23 : Nanoparticules fixées à un nanotube de carbone.
e. Réparation des connexions nerveuses
Une révolution majeure que proposent d’apporter les nanotechnologies est la réparation des connexions neuronales. En effet, jusqu'à aujourd’hui il est extrêmement difficile de refaire le contact entre deux nerfs sectionnés. En 1994, le Docteur Stéphane Woerly, Professeur l’université Laval à Québec a mis au point un hydrogel contenant des polymères et des précurseurs permettant la reconstruction partielle de la moelle épinière. Les essais se sont révélés positifs sur des animaux et n’ont pas encore été testés sur l’homme. Cependant, la moelle épinière ne retrouve pas sa structure d’origine au niveau de la jonction. La marche devient possible après plusieurs mois de convalescence mais reste difficile. Or un étudiant en doctorat de la Monash University a développé une nouvelle technique qui pourrait révolutionner le traitement des cellules souches dans la réparation des connexions nerveuses. Il a employé des fibres biodégradables de polymères existantes, 100 fois plus petites que des cheveux humains, et les a reconstruites pour créer un échafaudage unique qui pourrait permettre à des cellules souches de réparer les nerfs.
Le nano-échafaudage est injecté dans le corps à l'emplacement nécessitant la régénération nerveuse. Des cellules souches sont implantées dans la zone de cassure et adhèrent parfaitement à l'échafaudage et des nerfs se "tissent" progressivement dans cette nanostructure. Avec le temps, l'échafaudage se décompose et il est naturellement éliminé du corps, laissant les nerfs nouvellement régénérés intacts.

Fig. 24 : Echafaudage autour d'un nanotube de carbone.
Une autre étude proposerait d’utiliser un échafaudage en nanotubes de carbone pour un rendement encore meilleur. L’utilisation de ces véritables ponts entre les nerfs permettrait même de réparer des connexions de diamètre très réduit et d’être utilisé dans la régénération de certaines zones du cerveau.
Entrez dans le nanomonde...